Luigi Ricciardi 1 , Rosa Mazzeo 2,*© , Angelo RaffAele Marcotrigiano 1 , Guglielmo Rainaldi 3 , Paolo Iovieno 4 , Vito Zonno 1 , Stefano Pavan 1 © und Concetta Lotti 2,*
- 1 Institut für Boden-, Pflanzen- und Lebensmittelwissenschaften, Abteilung Pflanzengenetik und Züchtung Universität Bari, Via Amendola 165/A, 70125 Bari, Italien; luigi.ricciardi@uniba.it (LR);angelo.marcotrigiano@uniba.it (ARM); vito.zonno@uniba.it (VZ); stefano.pavan@uniba.it (SP)
- 2 Institut für Landwirtschafts-, Ernährungs- und Umweltwissenschaften, Universität Foggia, Via Napoli 25, 71122 Foggia, Italien
- 3 Institut für Biowissenschaften, Biotechnologien und Biopharmazeutika, Universität Bari, Via Orabona 4, 70125 Bari, Italien; guglielmo.rainaldi@uniba.it
- 4 Department of Energy Technologies, Bioenergy, Biorefinery and Green Chemistry Division, ENEA Trisaia Research Center, SS 106 Ionica, km 419+500, 75026 Rotondella (MT), Italien; paolo.iovieno@enea.it
* Korrespondenz: rosa.mazzeo@unifg.it (RM); Concetta.lotti@unifg.it (CL)
Abstract:
Zwiebel (Lauch cepa L.) ist die zweitwichtigste Gemüsepflanze weltweit und wird wegen ihrer gesundheitlichen Vorteile weithin geschätzt. Trotz ihrer bedeutenden wirtschaftlichen Bedeutung und ihres Wertes als funktionelles Lebensmittel sind Zwiebeln hinsichtlich ihrer genetischen Vielfalt kaum untersucht worden. Hier untersuchten wir die genetische Variation in der „Acquaviva red onion“ (ARO), einer Landsorte mit einer jahrhundertealten Anbaugeschichte in einer kleinen Stadt in der Provinz Bari (Apulien, Süditalien). Ein Satz von 11 Mikrosatellitenmarkern wurde verwendet, um die genetische Variation in einer Keimplasmasammlung zu untersuchen, die aus 13 ARO-Populationen und drei gängigen kommerziellen Typen bestand. Analysen der genetischen Struktur mit parametrischen und nicht-parametrischen Methoden haben gezeigt, dass die ARO einen gut definierten Genpool darstellt, der sich deutlich von den Landrassen Tropea und Montoro unterscheidet, mit denen sie oft verwechselt wird. Um Zwiebeln zu beschreiben, die normalerweise für den Frischverzehr verwendet werden, wurden der Gehalt an löslichen Feststoffen und die Schärfe bewertet, was eine höhere Süße im ARO im Vergleich zu den beiden oben genannten Landrassen zeigte. Insgesamt ist die vorliegende Studie nützlich für die zukünftige Valorisierung der ARO, die durch Qualitätssiegel gefördert werden könnte, die dazu beitragen könnten, kommerziellen Betrug einzuschränken und das Einkommen von Kleinbauern zu verbessern.
Einleitung
Die Gattung Allium umfasst etwa 750 Arten [1], unter denen die Zwiebel (Allium cepa L., 2n = 2x =16) eine der am weitesten verbreiteten ist. A. cepa hat einen zweijährigen Zyklus und ein sich auskreuzendes Fortpflanzungsverhalten. Heutzutage ist die weltweite Zwiebelproduktion (97.9 Mt) die zweitwichtigste Gemüsepflanze nach der Tomate [2]. Zwiebelknollen werden seit jeher sowohl als Nahrungsmittel als auch in der Volksheilkunde verwendet. Tatsächlich berichteten die alten Ägypter bereits in einem medizinischen Papyrus von 1550 v. Chr., dem Codex Ebers [3], über mehrere therapeutische Formeln, die auf der Verwendung von Knoblauch und Zwiebeln basieren.
Dieses vielseitige und gesunde Gemüse wird roh, frisch oder als verarbeitetes Produkt verzehrt und verwendet, um den Geschmack vieler Gerichte zu verbessern. Mehrere neuere Studien behaupten, dass der Verzehr von Zwiebeln das Risiko von Herz-Kreislauf-Erkrankungen [4,5], Fettleibigkeit [6], Diabetes [7] und verschiedenen Krebsarten [8–10] verringern kann. Die gesundheitsfördernden Eigenschaften von Zwiebeln werden oft hohen Konzentrationen von zwei Klassen nutrazeutischer Verbindungen zugeschrieben: Flavonoiden und Alk(en)ylcysteinsulfoxiden (ACSOs). Die erste Klasse umfasst Flavonole und Anthocyane. Quercetin ist das wichtigste nachweisbare Flavonol, das für seine starken antioxidativen und entzündungshemmenden Eigenschaften beim Abfangen freier Radikale und der Bindung von Übergangsmetallionen bekannt ist [11]; während Anthocyane einigen Zwiebelsorten eine rote/violette Farbe verleihen. Das am häufigsten vorkommende ACSO ist Isoalliin [(+)-trans-S-1-propenyl-L-cysteinsulfoxid] [12], eine in den Zellen gespeicherte, nicht flüchtige und nicht proteinogene Schwefelaminosäure, die indirekt für das scharfe Aroma und den Geschmack von Zwiebeln verantwortlich ist [13]. Bei Gewebezerstörung wird Isoalliin durch das Enzym Alliinase gespalten, um eine Reihe flüchtiger Verbindungen (Pyruvat, Ammoniak, Thiosulfonate und Propanethial-S-oxid) zu produzieren, die ein Reißen hervorrufen und einen unangenehmen Geruch (Scharfheit) verursachen. [14]. Die Zwiebelschärfe wird oft als die Menge an durch Hydrolyse erzeugter Brenztraubensäure pro Gramm Frischgewicht gemessen [15.16].
In den Ländern des Mittelmeerbeckens, vorgeschlagen als eines der Zentren der sekundären Vielfalt a. Belastung [17.18], Zwiebelknollen weisen eine große Variabilität in Form, Größe, Farbe, Trockenmasse und Schärfe auf [19-einer]. Darüber hinaus können Düngung auf Schwefelbasis, agronomische Praktiken, Art des Bodens, klimatische Bedingungen und der Genotyp von Sorten oder Landrassen die Zwiebelqualität beeinflussen, indem sie besondere organoleptische und Nährwerte verleihen [23-einer]. In Italien werden trotz der breiten Verfügbarkeit von Zwiebel-Keimplasma oft nur wenige Zwiebelsorten wissenschaftlichen Studien unterzogen und richtig charakterisiert [28.29].
Eine gründliche genetische und phänotypische Charakterisierung der Agrobiodiversität ist entscheidend, um eine angemessene Erhaltung der pflanzengenetischen Ressourcen sicherzustellen und die Verwendung spezifischer Genotypen in der Wertschöpfungskette zu fördern [30-einer]. Simple Sequence Repeat (SSR)-Marker wurden häufig für die Kartierung ausgewählt [33-einer], DNA-Fingerprinting und Sortendiskriminierung [36-einer], und zuverlässige Schätzung der genetischen Variabilität innerhalb und zwischen Landrassen [39-einer], da sie lokusspezifisch, multiallelisch, kodominant vererbt, hochgradig reproduzierbar und für eine automatisierte Genotypisierung geeignet sind.
In der vorliegenden Studie konzentrierten wir uns auf eine traditionelle apulische Landsorte, die „Acquaviva Red Onion“ (ARO), die nach biologischen Anbaumethoden in einem kleinen Gebiet der Stadt Acquaviva delle Fonti in der Provinz Bari angebaut wird (Apulien, Süditalien). Die Zwiebeln dieser Landrasse sind groß und abgeflacht und rot gefärbt und werden hauptsächlich in lokalen Rezepten verwendet. Obwohl die ARO das Qualitätszeichen „Slow Food Presidium“ erhalten hat, könnte ihre Produktion durch Qualitätszeichen der Europäischen Union wie geschützte geografische Angabe (ggA) und geschützte Ursprungsbezeichnung (g. U.) weiter gefördert und geschützt werden, da diese zur Begrenzung der Handelsbetrug und zur Verbesserung des Einkommens von Kleinbauern. Hierin wurden molekulare SSR-Marker als leistungsstarke Werkzeuge verwendet, um die genetische Variation zwischen ARO-Populationen zu bewerten und diese Landrasse von zwei anderen süditalienischen Landrassen für rote Zwiebeln zu unterscheiden. Darüber hinaus schätzten wir die Schärfe und den Gehalt an löslichen Feststoffen, um den ARO-Geschmack in Bezug auf die Marktnachfrage zu bewerten.
Die Ergebnisse
Einrichtung der Acquaviva Red Onion Keimplasma-Sammlung und morphologische Charakterisierung
Samen von 13 Populationen der ARO-Landrasse, die von Landwirten im Rahmen des BiodiverSO-Projekts Region Apulien gespendet wurden, wurden verwendet, um eine ARO-Keimplasmasammlung aufzubauen.
Morphologische Deskriptoren in Bezug auf Zwiebel, Haut und Fleisch wurden auf ARO-Keimplasma und auf drei Zwiebel-Landrassen gesammelt, von denen zwei zur Landrasse „Tropea Red Onion“ (TRO) und eine zur Landrasse „Montoro Copper Onion“ (MCO) gehören (Abbildung 1). Alle ARO-Zwiebeln waren flach und zeichneten sich durch rote Außenhaut und Fruchtfleisch mit unterschiedlichen Rotschattierungen aus. Im Gegensatz dazu war das Fruchtfleisch von TRO-Zwiebeln vollständig rot, während das Fruchtfleisch von MCO-Zwiebeln schwach pigmentiert war (Tabelle S1). Die biochemische Analyse ermöglichte die Bewertung des Gehalts an löslichen Feststoffen und der Schärfe. Wie in Tabelle angegeben 1, die Mittelwerte des Gehalts an löslichen Feststoffen von Zwiebeln in ARO-Populationen betrugen 7.60 und reichten von 6.00 (ARO12) bis 9.50° Brix (ARO11 und ARO13). Dieser Wert war höher als der für die Landrassen TRO und MCO geschätzte (4.25 bzw. 6.00° Brix).

Tabelle 1. Feststoffgehalt und Schärfewerte, bewertet in Populationen von „Acquaviva Red Onion“ (ARO), „Tropea Red Onion“ (TRO) und „Montoro Copper Onion“ (MCO) *.
| CODE | Löslicher Feststoffgehalt (Brix) | Schärfe (pMolg-1 FW) | ||
| Bedeuten | CV y (%) | Bedeuten | CV y (%) | |
| ARO1 | 6.25 D * | 5.65 | 5.84 ab * | 23.78 |
| ARO2 | 7.25 DC | 4.87 | 6.51 die | 22.98 |
| ARO3 | 7.50 BCD | 9.42 | 5.28 ab | 22.88 |
| ARO4 | 7.50 BCD | 0.00 | 6.97 die | 3.74 |
| ARO 5 | 7.50 BCD | 0.00 | 6.80 die | 9.68 |
| ARO6 | 6.25 D | 5.65 | 4.51 ab | 39.18 |
| ARO7 | 7.25 DC | 4.87 | 5.25 ab | 15.44 |
| ARO8 | 9.00 AB | 0.00 | 7.04 die | 3.49 |
| ARO9 | 8.25 ABC | 4.28 | 6.84 die | 0.15 |
| ARO10 | 7.00 DC | 0.00 | 5.94 ab | 6.57 |
| ARO11 | 9.50 A | 7.44 | 5.54 ab | 16.43 |
| ARO12 | 6.00 D | 0.00 | 4.91 ab | 9.70 |
| ARO13 | 9.50 A | 7.44 | 6.63 die | 24.93 |
| MCO | 6.00 D | 0.00 | 4.18 ab | 2.66 |
| TRO1 | 4.25 E | 8.31 | 2.80 b | 2.10 |
| TRO2 | 4.25 E | 8.31 | 4.28 ab | 4.79 |
* Mittelwerte mit denselben Buchstaben in Groß- oder Kleinschreibung unterscheiden sich statistisch nicht bei 0.01 P bzw. 0.05 P (SNK-Test). y Variationskoeffizient.
Der Mittelwert der ARO-Schärfe, bestimmt anhand des Brenztraubensäuregehalts, betrug 6.00 und reichte von 4.51 pmol g-1 FW (ARO6) bis 7.04 (ARO8). Dieser Wert war höher als der in TRO- und MCO-Landrassen geschätzte (3.54 pmol g-1 FW und 4.18 pmol g-1 FW bzw.).
SSR-Polymorphismus und genetische Beziehungen zwischen Akzessionen
In der vorliegenden Studie stellten 11 von 37 getesteten SSR-Primer-Kombinationen Single-Locus-Polymorphismen bereit, dh sie ergaben höchstens zwei Amplifikationsprodukte in einem einzelnen Individuum. Insgesamt wurden bei 55 Personen 320 Allele mit einer Anzahl von Allelen pro Locus von 2 (ACM147 und ACM 504) bis 11 (ACM132) und einem Mittelwert von 5 Allelen nachgewiesen (Tabelle 2). In einzelnen Populationen reichte die Anzahl der Allele (Na) von 1.94 (ACM147 und ACM504) bis 5.38 (ACM132), während die effektive Anzahl der Allele (Ne) von 1.41 (ACM152) bis 2.82 (ACM449) reichte. Abweichungen zwischen den Na- und Ne-Werten waren auf das Vorhandensein von Allelen mit geringer Häufigkeit in den Populationen und das Vorherrschen von nur wenigen Allelen zurückzuführen. Der höchste beobachtete Heterozygotiewert (Ho) wurde für ACM138 und ACM449 (0.62) hervorgehoben, während der niedrigste mit ACM152 (0.25) assoziiert war. Die erwartete Heterozygotie (He), die der theoretischen Erwartung in einer panmiktischen Population entspricht, reichte von 0.37 (ACM504) bis 0.61 (ACM132, ACM138 und ACM449). Der Wright-Fixierungsindex (Fis) zeigte für alle Marker Werte nahe Null (durchschnittlich 0.05), was auf ähnliche Werte zwischen beobachteten und erwarteten Heterozygotiegraden hinweist, wie für eine Auskreuzungsart erwartet. Die Effizienz einzelner SSR-Marker beim genetischen Fingerabdruck wurde durch den Index des polymorphen Informationsgehalts (PIC) mit einem Mittelwert von 0.48 geschätzt und reichte von 0.33 (ACM504) bis 0.67 (ACM132). Ein weiterer Effizienzindex, der Shannon's Information Index (I), zeigte einen Mittelwert von 0.84, und angenommene Werte lagen zwischen 0.45 (ACM152) und 1.20 (ACM132).
Tabelle 2. Polymorphismusmerkmale der 11 SSR-Marker, die zur Schätzung der genetischen Diversität in ARO-, TRO- und MCO-Populationen verwendet werden. Gesamtzahl der Allele (Na), Bandgrößenbereich und Index des polymorphen Informationsgehalts (PIC) Beziehen sich auf den Gesamtsatz von 320 Personen, die in dieser Studie genotypisiert wurden. Anzahl der Allele (Na), Anzahl der effektiven Allele (Ne), beobachtete Heterozygotie (Ho), erwartete Heterozygotie (He), Fixierungsindex (Fis) und Shannons Informationsindex (I) beziehen sich auf Mittelwerte, die aus 16 Populationen berechnet wurden, die jeweils aus 20 Individuen bestehen.
| Ort. | Gesamt Na | Größenbereich (bp) | PIC | Bedeuten | |||||
| Na | Ne | Ho | He | I | Fis | ||||
| ACM91 | 4 | 189-205 | 0.40 | 2.63 | 1.72 | 0.38 | 0.39 | 0.66 | 0.04 |
| ACM101 | 4 | 229-241 | 0.52 | 2.94 | 2.37 | 0.53 | 0.56 | 0.92 | 0.06 |
| ACM132 | 11 | 186-248 | 0.67 | 5.38 | 2.78 | 0.55 | 0.61 | 1.20 | 0.09 |
| ACM138 | 5 | 242-272 | 0.66 | 3.69 | 2.82 | 0.62 | 0.61 | 1.09 | -0.02 |
| ACM147 | 2 | 264-266 | 0.37 | 1.94 | 1.83 | 0.44 | 0.44 | 0.62 | -0.01 |
| ACM152 | 4 | 228-244 | 0.25 | 2.38 | 1.41 | 0.25 | 0.27 | 0.45 | 0.07 |
| ACM235 | 4 | 286-298 | 0.41 | 2.81 | 1.77 | 0.44 | 0.41 | 0.72 | -0.06 |
| ACM446 | 6 | 108-120 | 0.56 | 3.50 | 2.48 | 0.49 | 0.58 | 1.01 | 0.16 |
| ACM449 | 8 | 120-140 | 0.66 | 4.88 | 2.82 | 0.62 | 0.61 | 1.18 | -0.03 |
| ACM463 | 5 | 202-210 | 0.47 | 3.38 | 1.95 | 0.46 | 0.48 | 0.83 | 0.05 |
| ACM504 | 2 | 188-192 | 0.33 | 1.94 | 1.64 | 0.30 | 0.37 | 0.54 | 0.20 |
| Bedeuten | 5 | 0.48 | 3.22 | 2.15 | 0.46 | 0.48 | 0.84 | 0.05 |
Unter den Populationen zeigten ARO3, ARO6, ARO8, ARO10, TRO1 und MCO ein hohes Maß an genetischer Variation (Ho > 0.5), während die niedrigste Diversität in der Population ARO7 (Ho = 0.27) beobachtet wurde (Ergänzungstabelle S2). Insgesamt zeigten alle Akzessionen Fis Werte nahe Null (Fis Mittelwert = 0.054), wie unter zufälligen Paarungsbedingungen erwartet.
Analyse der molekularen Varianz und der genetischen Struktur
Die hierarchische Aufteilung der genetischen Variation zwischen und innerhalb von Populationen wurde von AMOVA berechnet. Die Ergebnisse zeigten einen beträchtlichen Teil der genetischen Variation innerhalb von Populationen (87 %). Die Variation zwischen den Populationen war mit 13 % hochsignifikant (P < 0.001) (Tabelle 3). Paarweise Werte des Fpt-Parameters, ein Analogon des Fst-Fixationsindex von Wright, die von 0.002 (ARO2/ARO10) bis 0.468 (ARO7/TRO2) reichten, waren signifikant (P < 0.05), mit Ausnahme von neun paarweisen Vergleichen (Ergänzungstabelle S3).
Tabelle 3. Analyse der molekularen Varianz von 320 Genotypen aus 16 Populationen von Allium cepa L.
| Quelle | df | Quadratsumme | Abweichungsschätzung | Abweichung (%) | Fpt | P |
| Unter Bevölkerungen | 15 | 458.63 | 1.16 | 13% | ||
| Innerhalb von Populationen | 304 | 2272.99 | 7.50 | 87% | 0.134 | 0.001 |
| Gesamt | 319 | 2731.62 | 8.66 |
Untersuchung der genetischen Struktur in der a. Belastung Die in dieser Studie genotypisierte Sammlung wurde mittels der auf dem Beimischungsmodell basierenden Clustering-Analyse durchgeführt, die in der Software STRUCTURE implementiert ist. Die Evanno-AK-Methode schlug eine Unterteilung in zwei Cluster (K = 2) als die informativste für unsere vor Datensatz,mit The weiter höchste peak bei k = 5 (ergänzende Rgure S1). Eine für K. = 2, ahpopulationen whier Arschigned auchnof die beiden Cluster mit ein Bernertoip-Koeffizient (q) > 0.7. Als shown rein Abbildung 2a, umfasste der erste Cluster (mit dem Namen S1) MCO- und alle ARO-Populationen, während der S2-Cluster die beiden TRO-Populationen gruppierte. Bei K = 5 bietet eine tiefere Beschreibung des Datensatzes (Abbildung 2b) wurden 75 % der Akzessionen einem der fünf Cluster zugeordnet. Die Trennung zwischen ARO (S1) und TRO (S2) wurde bestätigt, obwohl einige ARO-Populationen gemischt (q < 0.7) oder getrennt in den zwei neuen Clustern S3 und S4 (ARO7 bzw. ARO12) gruppiert wurden. Interessanterweise bildete der kommerzielle MCO-Typ einen deutlichen Cluster (S5), der von der apulischen roten Zwiebel getrennt war.
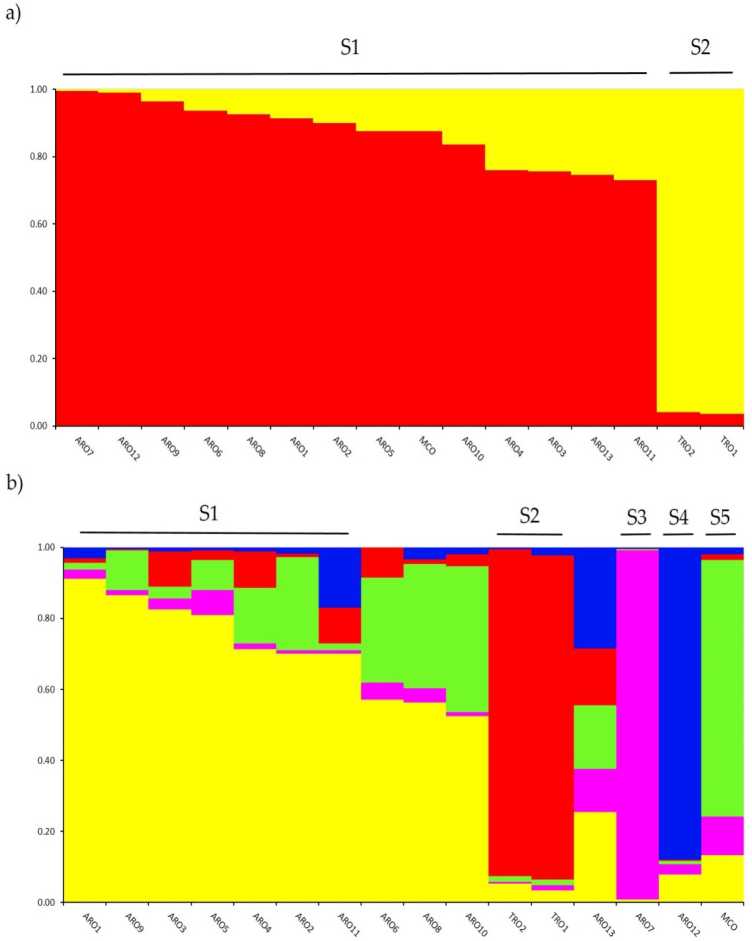
Genetische Beziehungen zwischen Populationen
Der SSR-Polymorphismus ermöglichte es, ein Dendrogramm der genetischen Vielfalt zu zeichnen, und die Ergebnisse der phylogenetischen Analyse sind in Abbildung gezeigt 3a. Hier wurde die Keimplasmasammlung in fünf Gruppen aufgeteilt, die stark von Bootstrap-Werten unterstützt wurden. Die ARO7- und ARO12-Populationen wurden sofort von den verbleibenden Populationen getrennt und bildeten zwei unterschiedliche Cluster. Der dritte Cluster umfasste die beiden kommerziellen Populationen von TRO, während der vierte Knoten MCO von elf ARO-Populationen trennte. Die zwischen den Populationen auftretende genetische Verwandtschaft wurde mittels Hauptkoordinatenanalyse (PCoA) weiter untersucht (Abbildung 3b). Wie bereits erwähnt, wurden die ARO-Populationen eng gruppiert, mit Ausnahme von ARO12 und ARO7, die in isolierten Positionen im PCoA-Diagramm auftauchten. Die beiden TROs und die MCO-Populationen waren im unteren rechten Bereich des Diagramms verstreut.
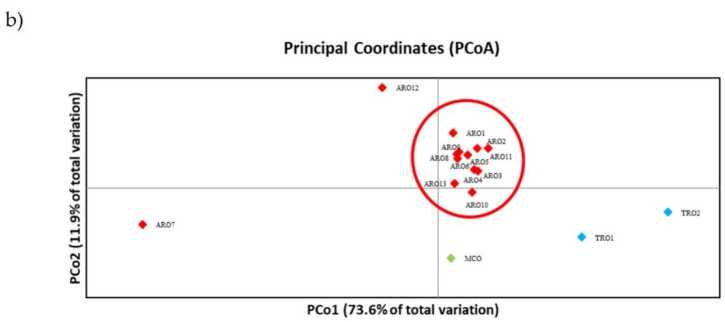
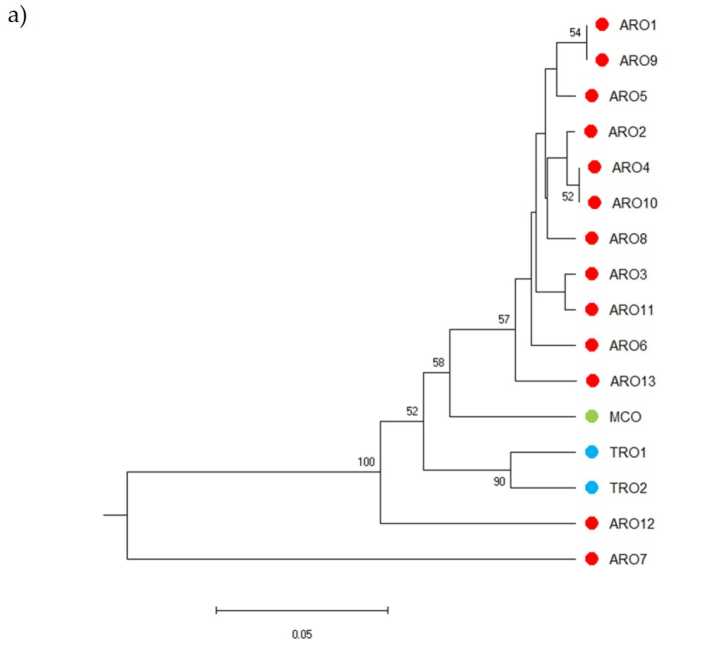
Abbildung 3. Genetische Vielfalt unter 16 a. Belastung Populationen, die in dieser Studie basierend auf ihrem SSR-Profil charakterisiert wurden. (a) UPGMA-Dendogramm der genetischen Distanz. Bootstrap-Unterstützungswerte >50 werden über den entsprechenden Knoten angezeigt; (b) Hauptkomponentenanalyse (PCoA). Der rot eingekreiste Cluster stimmte vollständig mit der Gruppe überein, die durch phylogenetische Analyse generiert wurde und aus 11 ARO-Akzessionen bestand.
Diskussion
Innerhalb der großen Menge an landwirtschaftlicher Biodiversität, die traditionell in Süditalien angebaut wird, stellen Zwiebel-Landrassen Nischenprodukte dar, die vor dem Risiko genetischer Erosion und der drohenden Verdrängung durch moderne Sorten bewahrt werden müssen. Im Rahmen des regionalen Projekts BiodiverSO, das darauf abzielt, genetische Ressourcen der Region Apulien zu sammeln, zu charakterisieren, zu fördern und zu schützen, die stark mit dem lokalen Erbe verbunden sind, haben wir eine Samensammlung von 13 Populationen der ARO-Landrasse angelegt. Wir berichteten über die erste Bewertung der ARO-Variation in Bezug auf DNA-Polymorphismen und zwei biochemische Parameter, Gehalte an löslichen Feststoffen und Brenztraubensäure, die mit Geschmacksmerkmalen in Zusammenhang stehen und für die Akzeptanz frischer ungekochter Produkte von Bedeutung sind. Außerdem wurden die Daten der ARO-Landrasse mit denen verglichen, die bei zwei anderen pigmentierten Zwiebellandrassen gesammelt wurden, mit denen sie oft verwechselt wurden.
Biochemische Analysen hoben die Süße der 13 ARO-Populationen hervor, verbunden mit einem hohen Gehalt an löslichen Feststoffen und mittlerer Schärfe, gemäß den Richtlinien der Süßzwiebelindustrie [31]. ARO-Zwiebeln waren süßer als die der TRO- und MCO-Landrassen und zeigten eine etwas höhere Schärfe. Die Süße in Zwiebeln ist jedoch auf ein Gleichgewicht zwischen Zuckergehalt und Schärfe zurückzuführen, daher könnte diese Charakterisierung nützlich sein, um die Auswahl wertvoller Genotypen zu unterstützen, die normalerweise von Landwirten nur auf der Grundlage der Morphologie durchgeführt wird.
Es wurde bestätigt, dass SSR-Marker ein nützliches Instrument zur Unterscheidung von Genotypen sind, obwohl sie in einem engen Anbaugebiet wie der Stadt Acquaviva delle Fonti gesammelt wurden. Die ausgewählten Marker zeigten eine höhere Anzahl von Allelen als die zuvor gemeldeten Marker [43] und [44], aber niedriger als die von gemeldeten Marker [45]. Darüber hinaus zeigten 50 % unseres Satzes von Markern PIC-Indexwerte von mehr als 0.5, was sich als geeignet erwies, die Populationen in der Sammlung zu diskriminieren, wie von vorgeschlagen [46]. Die Bewertung der Diversität innerhalb der Populationen ergab ähnliche Werte zwischen Ho und He, was zu einem niedrigen Fi führtes Werte. Dies steht im Einklang mit der Auskreuzungsnatur von A. cepa, die ernsthaft an Inzuchtdepression leidet [47]. Die Gesamt-Fis Der für Zwiebelpopulationen in dieser Studie berechnete Wert (0.054) war niedriger als der zuvor von [45] (0.22) und fast identisch mit dem von gefundenen [31] (0.08) und [48] (0.00), die die genetische Vielfalt bei Zwiebel-Landrassen aus Nordwestspanien bzw. Niger bewerteten. Bemerkenswerte Grade an Heterozygotie in ARO-Populationen bekräftigen die Vorstellung, dass Apulien ein Diversitätszentrum für viele Gartenbauarten darstellt [32, 42, 49-einer].
AMOVA betonte, dass die meisten molekularen Variationen in der in dieser Studie genotypisierten Sammlung innerhalb der Populationen liegen. Eine signifikante genetische Differenzierung zwischen Populationen (FPT Werte) zeigten das Auftreten einer genetischen Schichtung. Obwohl unsere Ergebnisse das Vorhandensein einer genetischen Einheitlichkeit in den meisten ARO-Populationen anzeigten, die einen gut definierten Cluster bildeten, zeigten die ARO7- und ARO12-Populationen tatsächlich ein deutlich unterschiedliches genetisches Profil. Dieses Ergebnis könnte auf eine unterschiedliche Herkunft des Saatguts zurückzuführen sein, das von den beiden Landwirten verwendet wurde, von denen die Populationen gesammelt wurden. Darüber hinaus kann die ARO-Landrasse aufgrund der erhaltenen Ergebnisse auf genetischer Ebene als eindeutig von den TRO- und MCO-Landrassen unterschieden werden. In einer aktuellen Studie [29] bewertete die genetische Vielfalt mehrerer italienischer Zwiebellandrassen, darunter „Acquaviva“, „Tropea“ und „Montoro“. Obwohl die Autoren SNP-Marker verwendeten, um die genetische Vielfalt einer breiteren Zwiebelsammlung zu bewerten, war die Genotypisierung nicht in der Lage, „Acquaviva“ von „Tropea“- und „Montoro“-Zwiebeln zu unterscheiden. Wahrscheinlich ist diese Diskrepanz auf den gefundenen niedrigen mittleren PIC-Wert (0.292) zurückzuführen, was auf eine bescheidene allgemeine Aussagekraft der analysierten Loci hindeutet, wie von behauptet [29]. Um das Vorhandensein von Unterstrukturen in ihrem italienischen Cluster zu untersuchen, wäre es außerdem besser gewesen, die italienischen Genotypen getrennt vom Rest der Sammlung zu analysieren. Wahrscheinlich hätte es erlaubt, Muster der genetischen Vielfalt in Verbindung mit geografischer Schichtung oder Merkmalen unter empirischer Selektion zu visualisieren.
Zusammenfassend stellt die vorliegende Studie einen umfassenden Bericht über eine Zwiebellandsorte dar, die mit dem lokalen Kulturerbe verbunden und für die Landwirte von wirtschaftlicher Bedeutung ist. Unsere Ergebnisse zeigen, dass ARO mit wenigen Ausnahmen durch einen gut definierten Genpool gekennzeichnet ist, der es verdient, vor dem Risiko einer genetischen Erosion bewahrt zu werden. Daher war der Aufbau einer repräsentativen Sammlung dieser wertvollen Quelle genetischer Vielfalt von entscheidender Bedeutung. Schließlich könnte die genetische und phänotypische Charakterisierung von ARO nützlich sein, um Qualitätszeichen von der Europäischen Union zu erhalten.
Materialen und Methoden
Keimplasmasammlung, Pflanzenmaterial und DNA-Extraktion
Eine Reihe von 13 Populationen der ARO-Landrasse wurde im Rahmen eines Projekts in der Region Apulien erworben (BiodiverSO: https://www.biodiversitapuglia.it/), durch eine Reihe von Missionen, die in „Acquaviva delle Fonti“, einer kleinen apulischen Stadt in der Provinz Bari, Italien, durchgeführt wurden. Die Sammelstellen der einzelnen Akzessionen wurden durch das Geographische Informationssystem (GIS) kartiert und in der Tabelle aufgeführt 4. Außerdem wurden zwei Populationen der TRO-Landrasse und eine Population der MCO-Landrasse in die vorliegende Studie aufgenommen und als Referenzen verwendet. Das gesamte Pflanzenmaterial wurde unter den gleichen Umgebungsbedingungen auf der Versuchsfarm „P Martucci“ der Universität Bari (41° 1'22.08″ N, 16°54'25.95″ E) unter Schutzkäfigen angebaut, um eine gegenseitige Bestäubung zu vermeiden Populationen und Gewährleistung der Bestäubung innerhalb der Population durch Schmeißfliegen (Lucilia Cäsar). Die 16 Populationen wurden nach Merkmalen im Zusammenhang mit Zwiebelgröße und -form sowie Haut- und Fleischfarbe charakterisiert (Tabelle S1). Zusätzlich wurde mit einem tragbaren Refraktometer eine Bestimmung des Gehalts an löslichen Feststoffen durchgeführt, und die Schärfe wurde in Zwiebelsaftproben unter Zugabe von 2,4-Dinitrophenylhydrazin (0.125 % v/v in 2 N HCl) und Bewertung der Extinktion bei 420 nm, wie von berichtet [31]. Der Duncan-Mehrbereichstest und der SNK-Test wurden durchgeführt, um das Vorhandensein signifikanter Unterschiede zu bestimmen.
Tabelle 4. Liste der in dieser Studie gesammelten und genotypisierten Populationen. Für jede Population werden der Identifikationscode, der lokale Name, die GPS-Koordinate und die Genbank, die das Saatgut bewahrt, gemeldet.
| Code | Name und Vorname | GPS Koordinaten | Genbank y |
| ARO1 | Cipolla rossa von Acquaviva | 40°54’21.708″ N 16°49’1.631” E | Di.SSPA |
| ARO2 | Cipolla rossa von Acquaviva | 40°53’14.28″ N 16°48’56.879” E | Di.SSPA |
| ARO3 | Cipolla rossa von Acquaviva | 40°54’11.304″ N 16°49’13.079” E | Di.SSPA |
| ARO4 | Cipolla rossa von Acquaviva | 40°54’3.348″ N 16°40’27.011” E | Di.SSPA |
| ARO5 | Cipolla rossa von Acquaviva | 40°51’59.76″ N 16°53’0.527” E | Di.SSPA |
| ARO6 | Cipolla rossa von Acquaviva | 40°52’48.72″ N 16°49’43.247” E | Di.SSPA |
| ARO7 | Cipolla rossa von Acquaviva | 40°53’13.47″ N 16°50’23.783” E | Di.SSPA |
| ARO8 | Cipolla rossa von Acquaviva | 40°53’18.816″ N 16°49’33.888” E | Di.SSPA |
| ARO9 | Cipolla rossa von Acquaviva | 40°54'51.372″N 16°49'3.504" E | Di.SSPA |
| ARO10 | Cipolla rossa von Acquaviva | 40°54’1.188″ N 16°49’24.311” E | Di.SSPA |
| ARO11 | Cipolla rossa von Acquaviva | 40°52'49.8″N 16°49'48.575" E | Di.SSPA |
| ARO12 | Cipolla rossa von Acquaviva | 40°52’38.892″ N 16°49’28.379” E | Di.SSPA |
| ARO13 | Cipolla rossa von Acquaviva | 40°53’21.768″ N 16°49’29.711” E | Di.SSPA |
| TRO1 | Cipolla Rossa Lunga von Tropea | - | Di.SSPA |
| TRO2 | Cipolla Rossa Tonda di Tropea | - | Di.SSPA |
| MCO | Cipolla Ramata von Montoro | - | Di.SSPA |
| y Di.SSPA, Institut für Boden-, Pflanzen- und Lebensmittelwissenschaften, Universität Bari. |
Blattmaterial von 20 Genotypen pro Population wurde entnommen und bis zur Verwendung bei -80 °C gelagert. Für polysaccharidreiche Arten, wie z A. cepa, Die ersten Schritte zur Entfernung von Polysacchariden sind unerlässlich, um DNA von guter Qualität zu erhalten, daher wurden anfängliche Waschschritte in STE-Puffer (0.25 M Saccharose, 0.03 M Tris, 0.05 M EDTA) wie in beschrieben durchgeführt [52]. Gesamt-DNA wurde nach dem CTAB-Verfahren extrahiert [53] und schließlich wurde es mit einem Nano Drop 2000 UV-Vis-Spektrophotometer (ThermoScientific, Waltham, MA, USA) und 0.8 % Agarose-Gelelektrophorese auf Qualität und Konzentration geprüft.
SSR-Analyse
16 EST-SSR Primerkombinationen entwickelt von [54] und zuvor in genetischen Diversitätsstudien von getestet [43] und [44] und 21 genomische SSR [45-einer] wurden gescreent, um ihre Eignung zu bewerten (Ergänzungstabelle S4). Die Genotypisierung wurde unter Verwendung des ökonomischen Fluoreszenz-Tagging-Verfahrens durchgeführt, bei dem der M13-Schwanz zu jedem Vorwärts-SSR-Primer hinzugefügt wird [56]. PCR-Mischungen wurden in 20-gL-Reaktionen hergestellt, die Folgendes enthielten: 50 ng Gesamt-DNA, 0.2 mM dNTP-Mischung, 1X PCR-Reaktionspuffer, 0.8 U DreamTaq-DNA-Polymerase (Thermo Scientific, Waltham, MA, USA), 0.16 gM Umkehrprimer , 0.032 gM Vorwärtsprimer, verlängert mit der M13-Sequenz (5'-TGTAAAACGACGGCCAGT-3'), und 0.08 gM eines universellen M13-Primers, der mit FAM- oder NED-Fluoreszenzfarbstoffen markiert ist (Sigma-Aldrich, St. Louis, MO, USA). Die PCR-Reaktionen wurden im Thermocycler SimpliAmp (Applied Biosystems, CA, USA) mit den folgenden Bedingungen für die Mehrzahl der Primerpaare durchgeführt: 94 °C für 5 min, 40 Zyklen bei 94 °C für 30 s, 58 °C für 45 s und 72 °C für 45 s und eine abschließende Elongation bei 72 °C für 5 min. Wie bei ACM446 und ACM449 wurde eine Touchdown-PCR mit Annealing von 60 °C bis 55 °C über 10 Zyklen, 30 Zyklen bei 55 °C, gefolgt von einer abschließenden Verlängerung von 5 min bei 72 °C, angewendet. PCR-Produkte wurden in eine Platte mit 96 Vertiefungen geladen und mit 14 gL Hi-Di-Formamid (Life Technologies, Carlsbad, CA, USA) und 0.5 gL GeneScan 500 ROX Size Standard (Life Technologies, Carlsbad, CA, USA) gemischt. Amplikons wurden mittels einer Kapillarsequenziermaschine ABI PRISM 3100 Avant Genetic Analyzer (Life Technologies, Carlsbad, CA, USA) aufgelöst, wobei die Allele als co-dominant bewertet und unter Verwendung der GeneMapper-Software Version 3.7 zugeordnet wurden.
Die Software GenAlEx 6.5 [57] und Cervus 3.0.7 [58] wurden verwendet, um die Anzahl der Allele (Na), die Anzahl der wirksamen Allele (Ne), die beobachtete Heterozygotie (Ho), die erwartete Heterozygotie (He), den polymorphen Informationsgehalt (PIC), den Shannon-Informationsindex (I) und den Fixierungsindex (Fis ) für jeden SSR-Locus.
Bewertung der genetischen Vielfalt
Die hierarchische Aufteilung der genetischen Variation zwischen und innerhalb der Zwiebelpopulationen wurde von GenAlEx 6.5 bewertet [57] durch die Analyse der molekularen Varianz (AMOVA) mit 999 Bootstrapping, um auf Signifikanz zu testen. Darüber hinaus wurde die GenAlEx 6.5-Software verwendet, um die Diversität innerhalb jeder Population abzuschätzen, indem der Durchschnitt von Ho, He und Fis über alle SSR-Loci berechnet wurde.
Die Populationsstruktur wurde durch den modellbasierten Bayes'schen Clustering-Algorithmus abgeleitet, der in der Software STRUCTURE v.2.3.4 implementiert ist [59]. Der Datensatz wurde mit einer Anzahl von hypothetischen Clustern (K) im Bereich von 1 bis 10 ausgeführt, wobei zehn unabhängige Läufe für jeden K-Wert festgelegt wurden. Mit dem Ziel, die Konsistenz der Ergebnisse zu überprüfen, wurden für jeden Durchlauf 100,000 initiale Burn-In-Perioden und 100,000 Iterationen der Markov Chain Monte Carlo (MCMC) unter dem Beimischungsmodell und unabhängigen Allelhäufigkeiten zwischen den Populationen durchgeführt. Der wahrscheinlichste K-Wert wurde unter Anwendung des AK-Verfahrens bestimmt, beschrieben durch [60], im webbasierten Programm STRUCTURE HARVESTER [61]. Eine einzelne Population wurde einem bestimmten Cluster zugeordnet, wenn ihr Zugehörigkeitskoeffizient (q-Wert) höher als 0.7 war, andernfalls wurde sie als gemischte Abstammung betrachtet.
Es wurde eine Hauptkoordinatenanalyse durchgeführt, um Muster der genetischen Verwandtschaft zwischen Akzessionen zu visualisieren, die durch die genetische Distanzmatrix von Nei (Ergänzungstabelle S5) offenbart wurden. Auf der Grundlage der Allelhäufigkeiten wurde ein Dendrogramm der genetischen Distanz erstellt, indem die ungewichtete Paargruppenmethode mit arithmetischen Mittelwerten (UPGMA)-Clusteranalyse in der POPTREEW-Software implementiert wurde [62]. Bootstrapping wurde angewendet, um das Vertrauen in hierarchisches Clustering zu bewerten, wobei 100 Resampling des Datensatzes eingestellt wurde. Endlich MEGA X-Software [63] wurde als Baumzeichnungssoftware verwendet.
Zusatzmaterialien: Die folgenden sind online verfügbar unter http://www.mdpi.com/2223-7747/9/2/260/s1. Tabelle S1: Morphologische Charakterisierung von ARO-, MCO- und TRO-Zwiebeln. Tabelle S2: Heterozygotie- und Fixierungsindizes, berechnet für ARO-Landrassen und TRO- und MCO-Landrassen. Tabelle S3: Paarweise Werte des Fpt-Parameters. Tabelle S4: Liste der in der Studie verwendeten SSRs. Tabelle S5. Paarweise Populationsmatrix der genetischen Distanz von Nei. Abbildung S1: Liniendiagramm der K-Werte, die sich mit Evannos Delta K ändern.
Autorenbeiträge: CL und LR konzipierten die Studie und gestalteten das Experiment; CL und PI führten eine molekulare Markeranalyse durch; ARM und VZ führten die Feldversuche durch; RM, SP, GR und CL waren an der Datenanalyse beteiligt; RM und CL schrieben das Manuskript. Alle Autoren haben die veröffentlichte Version des Manuskripts gelesen und sind damit einverstanden.
Finanzierung: Diese Arbeit wurde vom regionalen apulischen Projekt „Biodiversität apulischer Gemüsearten“ – Programma di Sviluppo Rurale per la Puglia 2014-2020 finanziert. Misura 10 – Sottomisura 10.2; Grant CUP H92C15000270002, Italien.
Danksagungen: Danksagung gebührt der „Azienda Agricola Iannone Anna“ und der „Associazione produttori della vera cipolla rossa di Acquaviva“ für die Bereitstellung von Pflanzenmaterial, das im Experiment verwendet wurde.
Interessenkonflikte: Die Autoren erklären keinen Interessenkonflikt.
Bibliographie
- 1. Stearn, WT Wie viele Arten von Allium sind bekannt? Kew Mag. 1992, 9180-182. [CrossRef]
- 2. FAOSTAT. Statistische Datenbank der FAO. Online verfügbar: http://www.fao.org/2017 (Zugriff am 8. Januar 2019).
- 3. Block, E. Die Chemie von Knoblauch und Zwiebel. Sci. Bin ich 1985, 252114-119. [CrossRef]
- 4. Lee, B.; Jung, JH; Kim, HS Bewertung von roten Zwiebeln auf antioxidative Aktivität bei Ratten. Lebensmittelchem. Giftig. 2012, 50, 3912-3919. [CrossRef]
- 5. Lee, SM; Mond, J.; Chung, JH; Cha, YJ; Shin, MJ Wirkung von Quercetin-reichen Zwiebelschalenextrakten auf arterielle Thrombose bei Ratten. Lebensmittelchem. Giftig. 2013, 57, 99-105. [CrossRef] [PubMed]
- 6. Yoshinari, O.; Shiojima, Y.; Igarashi, K. Anti-Adipositas-Wirkung von Zwiebelextrakt bei zuckerdiabetischen Fettratten. Nährstoffe 2012, 4,1518-1526. [CrossRef]
- 7. Akash, MSH; Rehmann, K.; Chen, S. Gewürzpflanze Allium cepa: Nahrungsergänzungsmittel zur Behandlung von Diabetes mellitus Typ 2. Ernährung 2014, 301128-1137. [CrossRef] [PubMed]
- 8. Wang, Y.; Tian, WX; Ma, XF Hemmende Wirkungen von Zwiebeln (Lauch cepa L.) Extrakt auf die Proliferation von Krebszellen und Adipozyten über die Hemmung der Fettsäuresynthase. Asien-Pazifik. J. Krebs Zurück. 2012,13, 5573-5579. [CrossRef] [PubMed]
- 9. Lai, WW; Hsu, SC; Chueh, FS; Chen, YY; Yang, JS; Lin, JP; Pfandrecht, JC; Tsai, CH; Chung, JG Quercetin hemmt die Migration und Invasion von humanen SAS-Mundkrebszellen durch Hemmung der NF-kappaB- und Matrix-Metalloproteinase-2/-9-Signalwege. Anticancer Res. 2013, 331941-1950. [PubMed]
- 10. Nicastro, HL; Ross, SA; Milner, JA Knoblauch und Zwiebeln: Ihre krebsvorbeugenden Eigenschaften. Krebs Zurück. Res. 2015, 8,181-189. [CrossRef]
- 11. Stärke, L.; Torricelli, P.; Boanini, E.; Gazzano, M.; Rubini, K.; Fini, M.; Bigi, A. Antioxidative und knochenreparierende Eigenschaften von Quercetin-funktionalisiertem Hydroxyapatit: Eine In-vitro-Kokulturstudie mit Osteoblasten-Osteoklasten-Endothelzellen. Acta-Biomater. 2016, 32, 298-308. [CrossRef]
- 12. Yamazaki, Y.; Iwasaki, K.; Mikami, M.; Yagihashi, A. Verteilung von elf Geschmacksvorläufern, S-Alk(en)yl-L-cystein-Derivaten, in sieben Allium-Gemüsen. Lebensmittelwissenschaft. Technol. Auflösung 2011, 17, 55-62. [CrossRef]
- 13. Block, E. Die Organoschwefelchemie der Gattung Allium – Implikationen für die organische Chemie von Schwefel. Angew. Chem.-Nr. Int. Hrsg. Engl. 1992, 311135-1178. [CrossRef]
- 14. Griffiths, G.; Trueman, L.; Crowther, T.; Thomas, B.; Smith, B. Zwiebeln – ein globaler Nutzen für die Gesundheit. Phytother. Auflösung 2002,16, 603-615. [CrossRef]
- 15. Schwimmer, S.; Weston, WJ Enzymatische Entwicklung von Brenztraubensäure in Zwiebeln als Maß für die Schärfe. J. Agric. Lebensmittelchem. 1961, 9, 301-304. [CrossRef]
- 16. Ketter, CAT; Randle, WM Beurteilung der Schärfe in Zwiebeln. In Geprüftes Studium für den Laborunterricht; Karcher, SJ, Hrsg.; Association for Biology Laboratory Education (ABLE): New York, NY, USA, 1998; Band 19, S. 177-196.
- 17. Hanelt, P Taxonomie, Evolution und Geschichte. In Zwiebeln und verwandte Pflanzen, Bd. I. Botanik, Physiologie und Genetik; Rabinowitch, HD; Brewster, JL, Hrsg.; CRC Press: Boca Raton, FL, USA, 1990; S. 1-26.
- 18. Rabinowitch, HD; Curra, L. Allium Crop Science: Jüngste Fortschritte; CABI Publishing: Wallingford, Großbritannien, 2002.
- 19. Mallor, C.; Carravedo, M.; Estopanan, G.; Mallor, F. Charakterisierung genetischer Zwiebelressourcen (Lauch cepa L.) vom spanischen Sekundarzentrum für Diversität. Spanne. J. Agric. Auflösung 2011, 9144-155. [CrossRef]
- 20. Ferioli, F.; D'Antuono, LF Bewertung von Phenolen und Cysteinsulfoxiden in lokalem Keimplasma von Zwiebeln und Schalotten aus Italien und der Ukraine. Genet. Ressource. Crop Evol. 2016, 63, 601-614. [CrossRef]
- 21. Petropoulos, SA; Fernandes, A.; Barros, L.; Ferreira, ICFR; Ntatsi, G. Morphologische, ernährungsphysiologische und chemische Beschreibung von 'vatikiotiko', einer lokalen Zwiebel-Landrasse aus Griechenland. Lebensmittelchem. 2015,182156-163. [CrossRef]
- 22. Liguori, L.; Adiletta, G.; Nazzaro, F.; Fratianni, F.; Di Matteo, M.; Albanese, D. Biochemische, antioxidative Eigenschaften und antimikrobielle Aktivität verschiedener Zwiebelsorten im Mittelmeerraum. J. Food Meas. Charakter 2019,131232-1241. [CrossRef]
- 23. Yoo, KS; Hecht, L.; Crosby, K.; Jones, R.; Leskovar, D. Unterschiede in der Zwiebelschärfe aufgrund von Sorten, Wachstumsumgebung und Zwiebelgrößen. Wissenschaft. Hortisch. 2006,110144-149. [CrossRef]
- 24. Beesk, N.; Perner, H.; Schwarz, D.; Georg, E.; Kroh, LW; Rohn, S. Verteilung von Quercetin-3, 4′-O-Diglucosid, Quercetin-4′-O-Monoglucosid und Quercetin in verschiedenen Teilen der Zwiebelknolle (Allium cepa L.) beeinflusst durch den Genotyp. Lebensmittelchem. 2010,122, 566-571. [CrossRef]
- 25. Caruso, G.; Conti, S.; Villari, G.; Borrelli, C.; Melchiona, G.; Minutolo, M.; Russo, G.; Amalfitano, C. Auswirkungen der Umpflanzzeit und Pflanzendichte auf Ertrag, Qualität und Gehalt an Antioxidantien bei Zwiebeln (Lauch cepa L.) in Süditalien. Wissenschaft. Hortisch. 2014,166111-120. [CrossRef]
- 26. Perez-Gregorio, MR; Regueiro, J.; Simal-Gandara, J.; Rodrigues, AS; Almeida, DPF Erhöhung des Mehrwerts von Zwiebeln als Quelle antioxidativer Flavonoide: Eine kritische Überprüfung. Kritisch Rev. Food Sci. Nutr. 2014, 54,1050-1062. [CrossRef] [PubMed]
- 27. Pohnl, T.; Schweiggert, RM; Carle, R. Einfluss der Anbaumethode und Sortenauswahl auf lösliche Kohlenhydrate und Scharfstoffe in Zwiebeln (Lauch cepa L.). J. Agric. Lebensmittelchem. 2018, 6612827-12835. [CrossRef] [PubMed]
- 28. Tedesco, I.; Carbone, V.; Spagnuolo, C.; Minasi, P.; Russo, GL Identifizierung und Quantifizierung von Flavonoiden aus zwei süditalienischen Sorten von Allium cepa L., Tropea (rote Zwiebel) und Montoro (Kupferzwiebel) und ihre Fähigkeit, menschliche Erythrozyten vor oxidativem Stress zu schützen. J. Agric. Lebensmittelchem. 2015, 63, 5229-5238. [CrossRef]
- 29. Villano, C.; Esposito, S.; Carucci, F.; Frusciante, L.; Carputo, D.; Aversano, R. Hochdurchsatz-Genotypisierung in Zwiebeln enthüllt die Struktur der genetischen Vielfalt und informative SNPs, die für die molekulare Züchtung nützlich sind. Mol. Züchten. 2019, 39 5. [CrossRef]
- 30. Mercati, F.; Longo, C.; Poma, D.; Araniti, F.; Lupini, A.; Mammano, MM; Fiore, MC; Abenavoli, MR; Sunseri, F Genetische Variante einer italienischen Tomate mit langer Haltbarkeit (Solanum lycopersicum L.) Sammlung anhand von SSR und morphologischen Fruchtmerkmalen. Genet. Ressource. Crop Evol. 2014, 62, 721-732. [CrossRef]
- 31. Gonzalez-Perez, S.; Mallor, C.; Garces-Claver, A.; Merino, F.; Taboada, A.; Rivera, A.; Pomar, F.; Perovic, D.; Silvar, C. Untersuchung der genetischen Vielfalt und Qualitätsmerkmale in einer Sammlung von Zwiebeln (Lauch cepa L.) Landrassen aus Nordwestspanien. Genetik 2015, 47, 885-900. [CrossRef]
- 32. Lotti, C.; Iovieno, P.; Centomani, I.; Marcotrigiano, AR; Fanelli, V.; Mimiola, G.; Summo, C.; Pavan, S.; Ricciardi, L. Genetische, bio-agronomische und ernährungsphysiologische Charakterisierung von Grünkohl (Brassica oleracea L. var. akzeptieren) Vielfalt in Apulien, Süditalien. Diversität 2018,10 25. [CrossRef]
- 33. Bardaro, N.; Marcotrigiano, AR; Bracuto, V.; Mazzeo, R.; Ricciardi, F.; Lotti, C.; Pavan, S.; Ricciardi, L. Genetische Analyse der Resistenz gegen Orobanche Crenata (Forsk.) in einer Erbse (Pisum sativum L.) Low-Strigolacton-Linie. J. Plant Pathol. 2016, 98, 671-675.
- 34. Wako, T.; Tsukazaki, H.; Yaguchi, S.; Yamashita, K.; Ito, S.; Shigyo, M. Kartierung quantitativer Merkmalsorte für die Schosszeit beim Bündeln von Zwiebeln (Lauch fistulosum L.). Euphytika 2016, 209, 537-546. [CrossRef]
- 35. Dhaka, N.; Mukhopadhyay, A.; Paritosh, K.; Gupta, V.; Pental, D.; Pradhan, AK Identifizierung genetischer SSRs und Konstruktion einer SSR-basierten Kopplungskarte in Brassica juncea. Euphytica 2017, 213, 15. [CrossRef]
- 36. Anandhan, S.; Splitter, SR; Gopal, J. Bewertung der Sortenidentität von Zwiebeln unter Verwendung von SSR-Markern. Saatgutwissenschaft. Technol. 2014, 42, 279-285. [CrossRef]
- 37. Mitrova, K.; Svoboda, P.; Ovesna, J. Die Auswahl und Validierung eines Markersatzes zur Unterscheidung von Zwiebelsorten aus der Tschechischen Republik. Tschechisch J. Genet. Pflanzenzucht. 2015, 51, 62-67. [CrossRef]
- 38. DiRienzo, V.; Miazzi, MM; Fanelli, V.; Sabetta, W.; Montemurro, C. Die Erhaltung und Charakterisierung der Biodiversität des apulischen Olivenkeimplasmas. Acta Hortic. 2018,1199,1-6. [CrossRef]
- 39. Mallor, C.; Arnedo-Andres, A.; Garces-Claver, A. Bewertung der genetischen Vielfalt des Spanischen Allium cepa Landrassen für die Zwiebelzüchtung unter Verwendung von Mikrosatellitenmarkern. Wissenschaft. Hortisch. 2014,17024-31. [CrossRef]
- 40. Rivera, A.; Mallor, C.; Garces-Claver, A.; Garcia-Ulloa, A.; Pomar, F.; Silvar, C. Bewertung der genetischen Vielfalt bei Zwiebeln (Allium cepa L.) Landrassen aus Nordwestspanien und Vergleich mit der europäischen Variabilität. NZJ Crop Hortic. 2016, 44103-120. [CrossRef]
- 41. DeGiovanni, C.; Pavan, S.; Tarent, F.; DiRienzo, V.; Miazzi, MM; Marcotrigiano, AR; Mangini, G.; Montemurro, C.; Ricciardi, L.; Lotti, C. Genetische Variation einer globalen Keimplasmasammlung von Kichererbsen (Cicer arietinum L.) einschließlich der von genetischer Erosion bedrohten italienischen Akzessionen. Physiol. Mol. biol. Pflanzen 2017, 23197-205. [CrossRef]
- 42. Mazzeo, R.; Morgese, A.; Sonnante, G.; Zuluaga, DL; Pavan, S.; Ricciardi, L.; Lotti, C. Genetische Vielfalt in Broccoli Rabe (Brassica rapa L. subsp. Sylvestris (L.) Janch.) aus Süditalien. Wissenschaft. Hortisch. 2019, 253140-146. [CrossRef]
- 43. Jakse, M.; Martin, W.; McCallum, J.; Havey, M. Einzelnukleotidpolymorphismen, Indels und einfache Sequenzwiederholungen zur Identifizierung von Zwiebelsorten. Marmelade. Soc. Hortisch. Wissenschaft. 2005,130, 912-917. [CrossRef]
- 44. McCallum, J.; Thomson, S.; Pither-Joyce, M.; Kenel, F. Genetische Diversitätsanalyse und Entwicklung von Einzelnukleotid-Polymorphismus-Markern in kultivierten Zwiebelzwiebeln basierend auf exprimierten Sequenz-Tag-Simple-Sequenz-Wiederholungsmarkern. Marmelade. Soc. Hortisch. Wissenschaft. 2008,133, 810-818. [CrossRef]
- 45. Baldwin, S.; Pither-Joyce, M.; Wright, K.; Chen, L.; McCallum, J. Entwicklung robuster genomischer Wiederholungsmarker für einfache Sequenzen zur Schätzung der genetischen Vielfalt innerhalb und zwischen Zwiebeln (Lauch cepa L.) Populationen. Mol. Züchten. 2012, 301401-1411. [CrossRef]
- 46. DeWoody, JA; Honeycutt, RL; Skow, LC Mikrosatellitenmarker in Weißwedelhirschen. J. Hered. 1995, 86, 317-319. [CrossRef] [PubMed]
- 47. Khodadadi, M.; Hassanpanah, D. Iranische Zwiebel (Lauch cepa L.) Sortenreaktionen auf Inzuchtdepression. Welt Appl. Wissenschaft. J. 2010,11, 426-428.
- 48. Abdou, R.; Bakasso, Y.; Saadou, M.; Baudoin, JP; Hardy, OJ Genetische Vielfalt von Niger-Zwiebeln (Lauch cepa L.) bewertet durch Simple Sequence Repeat Markers (SSR). Acta Hortic. 2016,1143, 77-90. [CrossRef]
- 49. Pavan, S.; Lotti, C.; Marcotrigiano, AR; Mazzeo, R.; Bardaro, N.; Bracuto, V.; Ricciardi, F.; Tarent, F.; D'Agostino, N.; Schiavulli, A.; et al. Ein ausgeprägter genetischer Cluster in kultivierten Kichererbsen, wie durch genomweite Markerentdeckung und Genotypisierung aufgedeckt wurde. Pflanzengenom 2017, 2017,10 [CrossRef]
- 50. Pavan, S.; Marcotrigiano, AR; Ciani, E.; Mazzeo, R.; Zonno, V.; Ruggieri, V.; Lotti, C.; Ricciardi, L. Genotypisierung durch Sequenzierung einer Melone (Cucumis melo L.) Keimplasmasammlung aus einem sekundären Diversitätszentrum hebt Muster genetischer Variation und genomischer Merkmale verschiedener Genpools hervor. BMC-Genom. 2017, 18 59. [CrossRef]
- 51. DiRienzo, V.; Sion, S.; Tarent, F.; D'Agostino, N.; Montemurro, C.; Fanelli, V.; Sabetta, W.; Boucheffa, S.; Tamendjari, A.; Pasqualone, A.; et al. Genetischer Fluss in der Olivenpopulation im Mittelmeerraum. Peer J. 2018, 6. [CrossRef]
- 52. Hirte, LD; McLay, TG Zwei Protokolle im Mikromaßstab zur Isolierung von DNA aus polysaccharidreichem Pflanzengewebe. J. Pflanzenres. 2011,124, 311-314. [CrossRef]
- 53. Doyle, JJ; Doyle, JL Isolierung von Pflanzen-DNA aus frischem Gewebe. Setzen Sie mit Achtsamkeit 1990,1213-14.
- 54. Kuhl, JC; Cheung, F.; Qiaoping, Y.; Martin, W.; Zewdie, Y.; McCallum, J.; Catanach, A.; Rutherford, P.; Waschbecken, KC; Jenderek, M.; et al. Ein einzigartiger Satz von 11,008 zwiebelexprimierten Sequenz-Tags zeigt exprimierte Sequenz- und Genomunterschiede zwischen den monokotylen Ordnungen Spargel und Poal. Pflanzenzelle 2004,16, 114-125. [CrossRef]
- 55. Kim, HJ; Lee, HR; Hyun, JY; Lied, KH; Kim, KH; Kim, JE; Hur, CG; Harn, CH Markerentwicklung für die genetische Reinheitsprüfung von Zwiebeln mit SSR Finder. Koreanische J. Rasse. Wissenschaft. 2012, 44, 421-432. [CrossRef]
- 56. Schuelke, M. Ein wirtschaftliches Verfahren zur Fluoreszenzmarkierung von PCR-Fragmenten. Nat. Biotechn. 2000, 18, 233-234. [CrossRef] [PubMed]
- 57. Peakall, R.; Smouse, PE GenAlEx 6.5: Genetische Analyse in Excel. Populationsgenetische Software für Lehre und Forschung: Ein Update. Bioinformatik 2012, 28, 2537-2539. [CrossRef] [PubMed]
- 58. Kalinowski, ST; Verjüngung, ML; Marshall, TC Die Überarbeitung, wie das Computerprogramm CERVUS Genotypisierungsfehler berücksichtigt, erhöht den Erfolg bei der Vaterschaftszuweisung. Mol. Ökologisch. 2007,161099-1106. [CrossRef]
- 59. Pritchard, JK; Stephens, M.; Rosenberg, NA; Donnelly, P. Assoziationskartierung in strukturierten Populationen. Bin. J. Hum. Genet. 2000, 67, 170-181. [CrossRef]
- 60. Evanno, G.; Regnaut, S.; Goudet, J. Erkennung der Anzahl von Personenclustern mit der Software STRUCTURE: A simulation study. Mol. Ökologisch. 2005,14, 2611-2620. [CrossRef]
- 61. Earl, D.; VonHoldt, B. STRUCTURE HARVESTER: Eine Website und ein Programm zur Visualisierung der STRUCTURE-Ausgabe und zur Implementierung der Evanno-Methode. Konserv. Genet. Ressource. 2011, 4. [CrossRef]
- 62. Takezaki, N.; Nei, M.; Tamura, K. POPTREEW: Webversion von POPTREE zum Konstruieren von Populationsbäumen aus Allelhäufigkeitsdaten und zum Berechnen einiger anderer Größen. Mol.-Nr. Biol. Entwicklung 2014, 31, 1622-1624. [CrossRef]
- 63. Kumar, S.; Stecher, G.; Li, M.; Knyaz, C.; Tamura, K. MEGA X. Analyse der molekularen Evolutionsgenetik über Computerplattformen hinweg. Mol.-Nr. Biol. Entwicklung 2018, 351547-1549. [CrossRef]