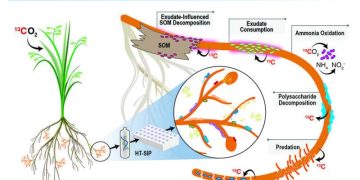
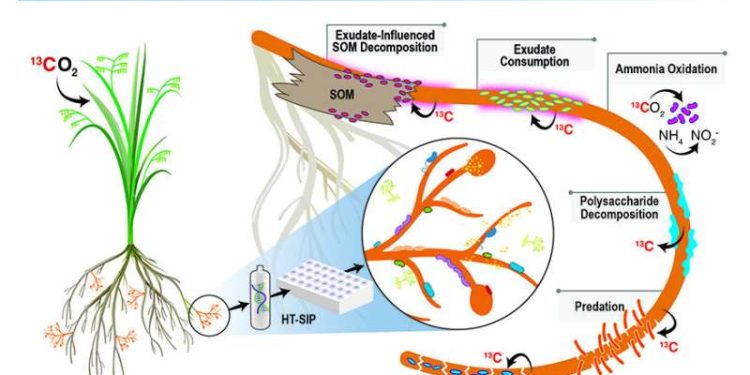
Die Forscher nutzten die neue High-Throughput Stable Isotope Sonding (HT-SIP)-Pipeline und Metagenomik, um einen ersten Einblick in das aktive Mikrobiom zu erhalten, das einen nützlichen Pflanzensymbionten, arbuskuläre Mykorrhizapilze (AMF), umgibt. Bildnachweis: Lawrence Livermore National Laboratory
Die Verknüpfung der Identität von Wildmikroben mit ihren physiologischen Merkmalen und Umweltfunktionen ist ein zentrales Ziel für Umweltmikrobiologen. Von den Techniken, die dieses Ziel anstreben, gilt das Stable Isotope Probing – SIP – als das effektivste für die Untersuchung aktiver Mikroorganismen in natürlichen Umgebungen.
Wissenschaftler des Lawrence Livermore National Laboratory (LLNL) haben eine neue Technik – Hochdurchsatz-SIP – entwickelt, die mehrere Schritte im Prozess der Untersuchung stabiler Isotope automatisiert und die Untersuchung der mikrobiellen Aktivität von Mikroorganismen unter realistischen Bedingungen ermöglicht, ohne dass eine Laborkultivierung erforderlich ist.
In SIP werden aktive Mikroben über den Einbau stabiler Isotope in ihre Biomasse identifiziert. Es gehört zu den leistungsstärksten Methoden in der mikrobiellen Ökologie, da es aktive Mikroben und ihre physiologischen Merkmale (Substratnutzung, zelluläre Biochemie, Stoffwechsel, Wachstum, Mortalität) in komplexen Lebensgemeinschaften unter natürlichen Bedingungen identifizieren kann.
Typischerweise erfordert das SIP-Verfahren erhebliche praktische Arbeit und ermöglicht nur eine kleine Anzahl von Proben. Aber die neue LLNL-Technik erfordert ein Sechstel der manuellen Arbeit im Vergleich zum manuellen SIP und ermöglicht die gleichzeitige Verarbeitung von 16 Proben.
„Unser halbautomatischer Ansatz verkürzt die Bedienerzeit und verbessert die Reproduzierbarkeit, indem er auf die arbeitsintensivsten Schritte von SIP abzielt“, sagte LLNL-Wissenschaftlerin Erin Nuccio und Hauptautorin eines Artikels, der in der Zeitschrift Microbiome erscheint. „Mit diesem Ansatz haben wir inzwischen über tausend Proben verarbeitet, darunter einige aus sehr wenig untersuchten Mikrohabitaten im Boden.“
Ein solcher Mikrohabitat ist der Boden, der das Gewebe der Mykorrhizae unmittelbar umgibt – eine Pilzart, die mit 72 % aller Landpflanzen symbiotische Beziehungen eingeht. Im Austausch gegen pflanzlichen Kohlenstoff versorgt der Pilz (arbuskuläre Mykorrhizapilze) seine Wirte mit lebenswichtigen Ressourcen wie Stickstoff, Phosphor und Wasser.
In dieser Proof-of-Concept-Studie zeigten die Autoren das „Nahrungsnetz“ von Wechselwirkungen, die durch Mykorrhizapilze im Boden stimuliert werden.
„Wir glauben, dass dies ein wichtiger Weg dafür ist, wie Pflanzenkohlenstoff breit im Boden verteilt wird. Der Boden enthält den größten Pool an aktiv zirkulierendem organischem Kohlenstoff auf dem Planeten“, sagte die Co-korrespondierende Autorin Jennifer Pett-Ridge, die LLNL-Projektleiterin und Leiterin des wissenschaftlichen Schwerpunktbereichs „Microbes Persist“ des Department of Energy für „Microbes Persist“ Soil Microbiome Scientific Focus Area . „Wir haben eine winzige Menge DNA sequenziert, die aktiven Organismen bestimmt und dann ihre Genome und mögliche Wechselwirkungen rekonstruiert.“
Andere LLNL-Autoren sind Steven Blazewicz, Marissa Lafler, Ashley Campbell, Jeffrey Kimbrel, Jessica Wollard, Rachel Hestrin sowie Forscher des Lawrence Berkeley National Laboratory, des DOE Joint Genome Institute und der University of California, Berkeley.